本文以西林瓶小容量注射剂无菌灌装生产线为例,在对所用隔离技术介绍的基础上,对不同布局方案提供说明、比较、评估和探讨。文中亦提及中国及欧盟GMP,和美国FDA及ISPE指南要求的房间洁净级别之间的差异,并提出相关建议。
概述
历史与发展
小容量注射剂无菌灌装线广泛应用于生物制药行业,其无菌环境和质量保证,与最终药品成品的质量休戚相关。无菌灌装生产技术从开放式生产到隔离技术的广泛采用,经历了从开放工作台到隔离操作器的发展历程。
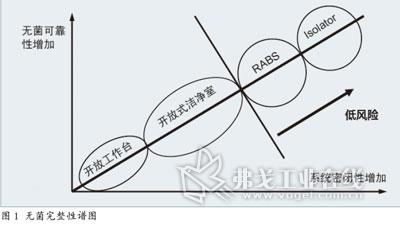
传统的开放工作台和开放式洁净室属于A级洁净室环境,由于没有将操作人员和产品严格分开,因此存在较大的无菌风险。RABS(限制进入屏障系统)和Isolator(隔离操作器)作为近十年来逐渐普及的隔离系统,在国际上已得到大量应用。随着新版中国GMP的施行,在无菌灌装方面使用隔离技术的要求日益明确。要实现新版GMP关于无菌灌装的要求,隔离化技术与隔离装备的应用是主要手段。
隔离操作器是在内部使用连续百级标准的清洁空气,并将内部和外部完全隔绝的物理装置。采用更严格的隔离标准,自控程度更好,设备操作台面全密闭,洁净风反复循环,因此其隔离功效更彻底。
对粉针生产所用冻干机来说,其本身是密闭空间,作为替代人工上料和下料的自动进出料系统,不仅提高生产速度,而且减少人为干预和出错可能性,目前已得到了普及。
设计原则
无菌生产线的设计应考虑以下诸多方面的因素。
满足无菌操作工艺和产品的需要。
采用RABS或隔离操作器技术都是无菌操作工艺的重要保证。对于高致敏性、毒性、抗肿瘤药、激素类或者高活性药物的分装,更需要最严格的隔离措施。

减少手动干预从而降低无菌生产过程中潜在的污染风险。
一般认为,人是洁净车间里的最大污染源。据统计,即使在最佳条件下,已更衣人员仍会释放出10000cfu/h或更多粒子到周围环境中。将人的干预降低到最少是技术发展的方向之一。
产品、操作人员和环境的交叉污染风险。
既要求保护操作人员和房间环境不受产品可能带来的污染,又要求保护产品不会受到来自人和房间环境带来的污染。

成本
无菌灌装生产线设备投入成本很大,并涉及到是否做在线清洗灭菌(CIP/SIP),是否采用100%称重,灌装精度控制等方面,洁净室的级别和空间大小等也对生产运行成本带来影响。
符合法律法规的要求。
除中国GMP之外,是否遵循欧盟GMP,以及美国FDA法规要求,也可能对布局和生产环境要求产生差异。本文的案例中将涉及这方面的讨论。
“过保护”
过保护概念指的是设计标准高于规范要求。虽然过保护设计会提高成本,但是在基于具体生产要求和风险评估的基础上,适当提高设计标准是控制污染、提高质量和降低风险的良好措施。
不同的法规要求
中国新版GMP
中国新版GMP无菌附录一第7条指出,应当根据产品特性、工艺和设备等因素,确定无菌药品生产用洁净区的级别。每一步生产操作的环境都应当达到适当的动态洁净度标准,尽可能降低产品或所处理的物料被微粒或微生物污染的风险。第13条中关于无菌灌装的条款见表1。
对于隔离操作器,中国新版GMP在第四章第十四条提及,隔离操作器所处环境的级别取决于其设计及应用。无菌生产的隔离操作器所处环境的级别至少应为D级。
欧盟GMP
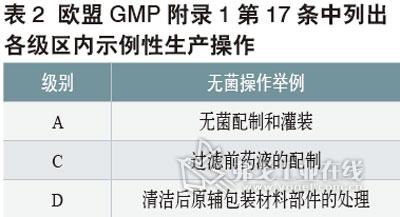
欧盟GMP(2008/11修订版)附录1无菌指南相关条款和上述中国新版GMP是一致的,第17条中列出了各级区内示例性生产操作,见表2。
关于隔离操作器,欧盟GMP无菌附录一第23条也指明,用于无菌生产的隔离操作器环境应受控并至少为D级。
美国FDA cGMP
在美国FDA cGMP(2004年9月版)无菌药品生产指南第四节厂房和设施 B 洁净支持区域部分的条文中提到:在洁净支持环境中所执行操作的特性决定了该区域的级别。FDA建议把直接毗邻无菌生产线的区域至少达到动态10000级(ISO 7)。制造商也可以定义该区域为1000级(ISO 6)或者维持整个灌装区为100级(ISO 5)。对于次关键区域例如设备清洗区,100000级(ISO8)是适当的设置。

同样在在该指南附录1第二部分设计篇中第4条中提到:考虑到隔离器设计和生产条件等因素,100000级(ISO 8)背景比较常见。无菌生产用隔离器不允许设置于无级别房间。
ISPE无菌指南
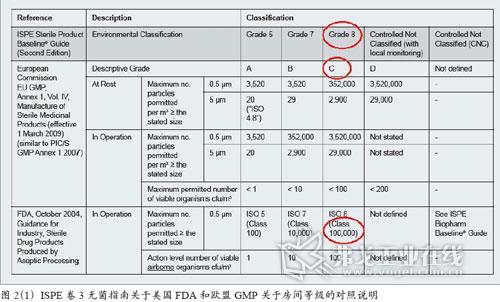
在ISPE(国际制药工程协会)于2011年9月刚更新并出版的ISPE卷3无菌指南第二版。该指南提供了美国FDA和欧盟GMP关于房间等级的明确对照,见图2(1)。通过对比看出,FDA只有动态(In Operation)概念,FDA所指100000级,与此等同的欧盟GMP洁净级别为C级,且FDA未定义相应的D级。在该指南表2-4中,也明确而详细地界定了无菌生产线各辅助房间的洁净级别,见图2(2)。值得注意的是,瓶具最终淋洗、灭菌和进入除热原隧道均被定义为Grade 8,所对应的中国和欧盟GMP洁净级别为C级。
关于隔离操作器,在9.2.1隔离操作器章节对隔离操作器进行了定义。其中正压封闭型式隔离操作器的环境定义为Grade 8,亦即中国和欧盟GMP的C级,见图2(3)。
多种布局方案
本文采用简单明了的图示,相关的配液、终端过滤、更衣区、洁净暂存、设备清洗灭菌等辅助设施已省略,这些配套设施也会影响布局,但灌装线更为核心,值得优先考虑。基于通用性考虑,采用粉针和水针两用生产线,通过输送线的方向切换来完成两种类型产品的切换。冻干机进出料部分均为自动进出料系统,RABS在无特殊生产工艺要求的情况下均采用开放式RABS。对于灌装机来说还有一个假定,即操作面和维修、装配设置在不同侧,这种设置应该是目前灌装机的主流。
基本布局
直线型灌装线,采用O-RABS,核心受控区为B+A,这是今后若干年内无菌小容量注射剂生产最多可能采用的方式,所以这里称之为基本布局,见图3(1)。
灌装生产线、输送轨道和冻干机进出料均在B级区,洗瓶和除热原隧道烘箱在D级区,轧盖设置在C级区。冻干机则在无级别区。
在该方案中,需3个更衣进出口。在1和2区之间,可以设置翻板或推门以节省一套更衣设施,只在停止灌装生产时打开同行,返回后重新生产前应该对环境重新做一次消毒和确认。
该方案为直线型,流线清晰,很适合供参观和展示,并且完全符合中国和欧盟GMP的定义。
借用轧盖间作通道
轧盖间与灌装间分隔,但有门联通这两个房间。这一布局在国内并不常见。
在该方案中,轧盖间也设置于B级区,该设计好于规范的要求,显然更为核心的灌装间应保持与轧盖间的正压差,见图3(2)。
需要2个更衣进出口,在1和2区,但如前述,也可以设置翻板或者推门以节省一个更衣区,只在停止灌装生产时打开同行,返回后生产前应对环境做消毒和确认。
这个方案体现了一种人流物流通道的变通性,进出B级区域的更衣区有所减少。人员在相同级别的灌装间和轧盖间之间的联系得到改进,无需频繁更换B级或C级洁净服。西林瓶的输送轨道穿过同级别房间,在特殊密封处理的要求方面有所降低和简化。
轧盖区由常规的C级变为B级,好于规范的要求,鉴于中国GMP(无菌附录第13条)所提未已加塞未轧盖的药瓶仍然处于未完全密封状态,并且2009年4月的GMP专家讨论稿也曾经要求轧盖工艺在B+A环境下进行,只是在2010年GMP正式版中又退了一步,提出可在C+A或D+A进行。因此这个方案其实有一些参考价值。
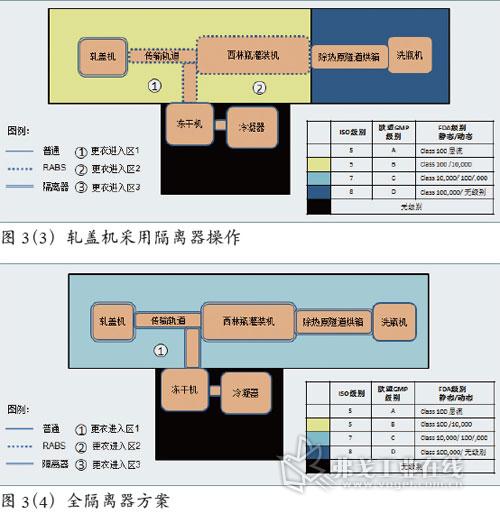
轧盖机采用隔离器操作
这一方案与方案二有一些类似。但是轧盖机和灌装机直接放在同一个B级房间。通过采用隔离器,试图避免轧盖过程中粉尘对环境带来的污染风险,见图3(3)。
在更衣区方面的考虑和前一个方案一致。
在此方案中,轧盖粉尘的在设备内部的控制、铝盖送入以及轧盖后瓶子的快速顺畅出料等方面都需要设备厂商进行优化考虑。
全隔离器方案
在这个方案中,对从除洗瓶机之外整条灌装生产线采用隔离操作器。整个背景至少保持D级环境,见图3(4)。
隔离操作器的采用,本身也更适用于前述的激素类、高致敏性、毒性类的产品,由于隔离器的隔离保护较RABS更彻底,因此对高附加值、高质量要求的产品来说也是较好的选择。
由于所有设施均在一个房间,在生产方面具有很好的联通性。通过对环境要求的降低,也节约了能耗和运行成本。
在环境控制和相互影响方面,例如除热原隧道烘箱带来热量的发散、从房间抽取空气带来的新风补充问题,以及洗瓶机带来的湿度控制问题等,需在设计中妥善考虑,但不在本文的讨论范围。
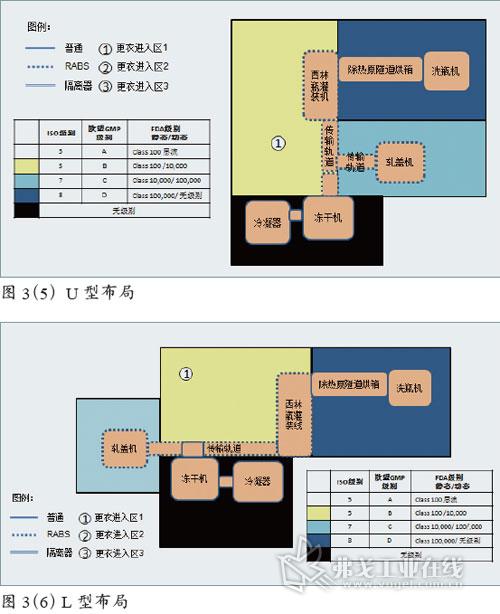
U型布局
U型布局在国内较常见,因其生产线外形近似U型而得名,见图3(5)。
在此方案中,空间的节省是其明显的优势。B级洁净室只需一个更衣区进出即可。不过,在灌装机的维修一侧在层流保护下作检修或者拆换泵等操作仍存在潜在的污染风险。
L型布局
L型布局在国内也很常见。与U型布局相似,空间的节省也是其明显的优势。B级洁净室只需一个更衣区进出即可,见图3(6)。不过在灌装机的维修一侧在层流保护下作检修或者拆换泵等操作仍存在潜在的污染风险。
随着技术进步,个别进口灌装机设备已经支持在操作面同一侧实现换泵操作,但大多数厂商设备还不能达到这样的目标。如采用CIP(Clean In Place在线清洗) 方式,则可进一步减少拆装带来的不便。从D区对灌装线进行维修,除设层流罩提供层流保护外,每次都需要对灌装机设施重新确认。
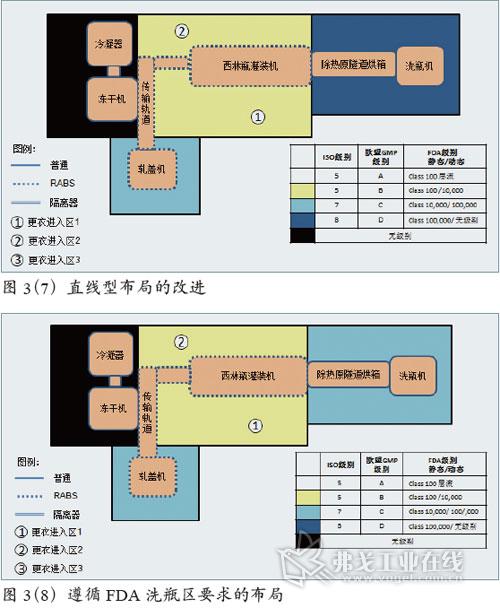
直线型布局的改进
直线型布局可以得到一些改进。与基本型相比,精简了一个需更衣进入的区域,见图3(7)。在该方案中,需要两个更衣进出口。在1和2区,也可以设置翻板或者推门以节省一个更衣区,只在停止灌装生产时打开同行,返回后生产前应对环境做消毒和确认。
遵循FDA洗瓶区要求的布局
方案见图3(8),洗瓶间被定义为C级,这和国内传统设计存在很大出入,容易引发争议。在前文中,已对FDA和ISPE关于洗瓶间和清洗/灭菌间的房间级别的C级要求已有摘录和分析。对于未来可能需要申报FDA的项目,洗瓶间和清洗/灭菌间应确定采用C级设计。即使项目不申报FDA认证,鉴于ISPE指南往往代表了制药行业的发展方向,将洗瓶间和清洗/灭菌间定义为C级仍是值得考虑或推荐的。
小结
生产设备和设施厂商技术的发展不会停止,如同生产商对药品质量的追求不会停止一样,与此同时,在工程设计方面的方案改进和设计优化同样需要不断改进。产品是不同的,厂房环境是不同的,所以布局也应该随变而变,在设计中需要追求最优化方案。本文旨在抛砖引玉,相信还有很多细节值得更多探讨和论证。