药液的配制工艺过程是,将药品的主药和辅料称量后溶解在适当的溶剂中,使其完全溶解。配制用的溶剂通常为水或含有部分有机溶剂的混合液。
1药液配制的原理和步骤
药液配制是将单组分或多组分的固体或液体药物,按照药物处方的要求均匀地溶解混合在液体中。
药液的配制步骤是在水或含有部分有机溶剂的混合液中,将主药完全溶解,通常需要辅之于搅拌,然后检测后调整溶液的药物含量和其他理化指标后待滤。
2溶解配制装置
配制药液所需容器、管道均采用316L不锈钢材料制造,表面粗糙度应尽量小(如Ra<0.45μm),便于清洗处理。配制药液所需容器、管道类必须进行清洁和蒸汽灭菌,配制容器上的计量器具(温度计、压力计、液位计等)必须满足耐灭菌高温和化学品的腐蚀。
3影响药液配制的主要因素
(1)药液的配制不仅对药物制剂是重要的而且和冻干工艺有关。例如,在低温下产品的低温热性能的偏差是和配方的变动直接有关。又例如,配制之前工艺水温的升高可能会引起水中聚团大小在分布上的变化,因而导致药液性质缺乏恒定性。
(2)除了温度之外,配制过程中的主要偏差原因是主药成分和辅料的浓度,最后成品的pH和调整所用的材料性质和数量以及配制期间溶液上方的气体的性质和压力,药液配制混和期间的热辐射能量,药液混合容器的材料成分以及药液配制时间等等。
(3)配制是处于冻干产品的关键性地位,因此确定配方中的关键参数是极其重要的,参数的数量和配制工艺的实质和置信度的期望值有关。
(4)需注意,溶配药液所需容器、管道类必须进行清洁和蒸汽灭菌。
4药液配制过程中管理确认的内容
配制过程中,针对不同药物的特殊要求,需要对溶解配制罐的各种参数进行调节控制:(1)温度进行调节(工艺用水温度、冷却水温度,药液温度等);(2)溶解过程调节(药液的溶解状态、pH、惰性气体的浓度、搅拌力等);(3)药液输送(压力、流量等);(4)药液过滤(过滤差压、流量);(5)pH调整(pH值、测量液温度);(6)流量调整。
5配制过程中的质量控制
配制过程中的质量控制:(1)溶解,药物的溶解状态、药液活性成分的含量、药液的pH值、异物等;(2)药液中的杂质过滤:控制异物和微粒子为主;(3)pH值的调整;(4)液量的调整:溶解状态、含量、pH、过滤器的确认试验、异物和其他杂质。
6配制装置的清洗和灭菌
配制结束后,应及时对配制装置进行清洗和灭菌。清洁和未清洁的器具分别按区域存放。配制后的处理内容如下:(1)配制结束后采用根据不同的工艺要求和清洁对象,采用注射用水、纯化水等工艺用水进行洗涤;(2)需要确定配制装置清洗后残留药液的确认方法和标准;(3)需要确定配制装置清洗后的灭菌方法(高压蒸汽灭菌、流通蒸汽灭菌、热水80℃以上的巴氏消毒等);(4)需要预设配制装置灭菌后的微生物数量的确认和合格的标准;(5)配制装置清洗灭菌的频率要求等,通常应规定每日进行一次。
7药液配制工艺单元
物料混合配制的目的是将分散的产品、辅料、溶剂集中起来,有可能是简单的液体混合,固体活性物质的溶解,也可能是包括更复杂的操作均质乳化或形成脂质体。对于水溶性药物处方,应尽可能的采用注射用水作为药物的溶剂。通常药液配制工艺单元的设置应注意点:
(1)物料混合之前,所使用的容器具和组件均应有效的清洁和消毒灭菌,以减少生产工艺中,下游工艺的生物负载和内毒素负荷。
(2)配制工艺由于有药物的活性成分可能会暴露在生产环境中,应特别注意空气中粉末的控制。配药工序空气的洁净级别应视生产过程的自动化程度和产品的特殊情况而定。
(3)由于冻干药品生产是非最终灭菌的无菌药品生产过程,冻干产品不能够进行灭菌或除菌过滤(例如无菌粉末注射剂),其配料过程应在背景环境为100,000级,环境为100级的条件下进行。如果,药品能够进行灭菌或除菌过滤,易生长微生物的无菌产品或最终灭菌产品,应在背景环境为100,000级洁净度条件下进行。
7.1药液的配制方式
药液配制通常有三个基本步骤,即原辅料称量、液体溶解配制、过滤除菌除杂质。图1为一常见的药液配制系统简图,图示药液配制的程序通常是:
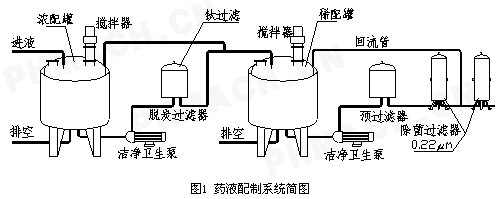
(1)加料溶解搅拌均匀。先按照药品处方要求,注入定量的注射用水至浓配罐内,然后将药物的活性成分和辅料,按处方称量后加入浓配罐内,在规定的温度条件下搅拌溶解均匀。这个过程中,通常还会加入适量的活性炭,搅拌均匀后静置一段时间。
(2)过滤。使用卫生级洁净输送泵或压缩空气将浓配后的液体,压滤通过杂质过滤器(通常用钛质的过滤器),经过脱炭处理后的滤液进入稀配罐内进行定量配制和含量、pH、杂质等半成品控制参数的检测。
(3)药液转移分装。达到药品的最终质量要求的液体通过洁净卫生泵或压缩空气将其过滤至分装设备进行分装,或由处于无菌操作区域内的无菌药液接受容器暂存待分装。
7.2两类药液配制系统的使用
一般无菌药品的配制系统设置按药液过滤与灌装的关系分为两种:
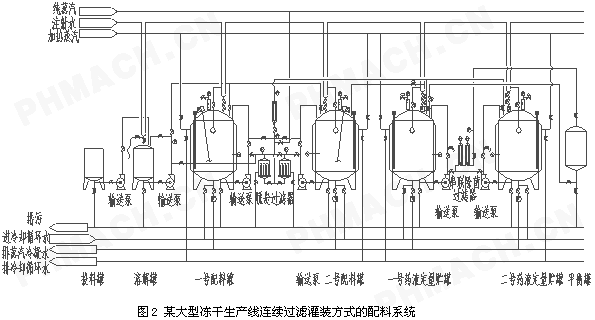
(1)连续过滤灌装方式的配料系统。通常,生产规模较大的冻干生产线采用此种系统设计。该配料系统能适应边过滤,边药液灌装的生产形式。其特点:规模较大、过滤器只能考虑在线地进行其完整性测试,并且需要在药液输送管道上串联配置两个相同孔径的除菌过滤器,以避免过滤过程中滤膜穿孔破坏的风险。图2为某大型冻干生产线连续过滤灌装方式的配料系统示意图。
(2)间隙过滤灌装方式的配料系统。此种灌装方式的配料系统主要使用在中、小规模的冻干生产线上,该配料系统中药液配置过程与药液输送管道平时处于分离的状态。药液配制完成后,通过有机硅橡胶等材料制成的软管输送至无菌操作区域内的药液接受容器中。其特点: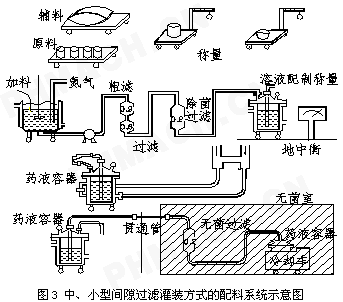 除菌过滤器需要完整性测试合格后对药液过滤,过滤完成后再次完整性测试合格才能够将本批药液用于灌装。这种系统较连续系统的最大优点是生产安排灵活,管道内残留很小,特别适合药物活性成分贵重,批量小的情况。图3为中、小型间隙过滤灌装方式的配料系统示意图。
除菌过滤器需要完整性测试合格后对药液过滤,过滤完成后再次完整性测试合格才能够将本批药液用于灌装。这种系统较连续系统的最大优点是生产安排灵活,管道内残留很小,特别适合药物活性成分贵重,批量小的情况。图3为中、小型间隙过滤灌装方式的配料系统示意图。
 除菌过滤器需要完整性测试合格后对药液过滤,过滤完成后再次完整性测试合格才能够将本批药液用于灌装。这种系统较连续系统的最大优点是生产安排灵活,管道内残留很小,特别适合药物活性成分贵重,批量小的情况。图3为中、小型间隙过滤灌装方式的配料系统示意图。
除菌过滤器需要完整性测试合格后对药液过滤,过滤完成后再次完整性测试合格才能够将本批药液用于灌装。这种系统较连续系统的最大优点是生产安排灵活,管道内残留很小,特别适合药物活性成分贵重,批量小的情况。图3为中、小型间隙过滤灌装方式的配料系统示意图。7.3药液的计量
液体可用流量计以容积定量的原理进行计量,但是,目前冻干药品生产工艺的趋势是采用重量分析方法来控制定量。在大规模生产时,将配料容器放置在电子称量衡器上或地中衡(地磅)上面。对任何一种计量的方法,都应该注意附着的电缆和连接管道对称量范围精确度和线性误差的影响。
7.4配料交叉污染的控制
配料时应仔细充分的考虑物料的交叉污染趋势。即在同一个生产车间内,前一批物料的残留可能会转移到下一批物料中,带来混药的污染风险。对不同产品车间,不同产品的平行配药以及上一批不同产品物料残渣也会有导致交叉污染风险的可能。
在配制系统的设计中,应有措施能有效处理交叉污染,包括物理和化学方式处理,以及对产品采取隔离和大范围的清洁处理。
恰当的通风系统可以有效地防止洁净室内空气中药物粉尘带来的交叉污染风险。排除粉末和活性成分残留污染的方法和配制设备(如反应罐、配料罐、搅拌装置、铲子、称量容器,离心泵以及真空泵等)的清洁净化,清洁净化的操作方法(在线清洗或离线清洗、在线灭菌或离线灭菌,物理灭菌或化学消毒等)均应包含在配制工程的设计之中。