摘 要:通过热分布的试验、生物指示剂试验来验证YX208B型手提式不锈钢蒸汽消毒器消毒运行状况、性能情况,并通过生产模拟实验,最后确定灭菌条件为121 ℃、30 min。
关键词:手提式;不锈钢蒸汽消毒器;验证
YX208B型手提式不锈钢蒸汽消毒器是医疗卫生、科研单位的通用灭菌设备,主要用于培养基、玻璃器皿、无菌工作服等的消毒灭菌。根据GMP(98版)第57条、58条规定药品生产的关键设备需验证[1],药品《认证检查标准》也规定关键设备的验证内容应包括灭菌设备[2],对药品生产中灭菌所用的YX208B型手提式不锈钢蒸汽消毒器应进行验证, 以确保物料灭菌符合规定要求。
设备验证包括预确认、安装确认、运行确认和性能确认。本次主要通过热分布试验、生物指示剂试验来验证该设备运行能否达到灭菌要求。
1 验证材料与方法
1.1 仪器与材料
(1)手提式不锈钢蒸汽消毒器(YX208B型,上海三申医疗器械有限公司);留点温度计(上海宜川仪表厂);嗜热脂肪芽孢杆菌指示剂(福建省药检所)。
(2)温度探头的筛选,实验所用的温度计均由福建省计量检验所检定合格后投入使用。
1.2 热分布测试
热分布测试目的:检查灭菌器箱腔内的热分布情况,检查箱腔内可能存在的冷点。
1.2.1 空载热分布实验
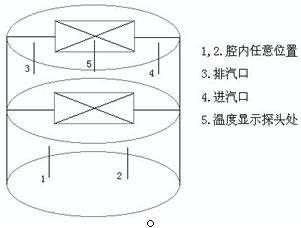
将灭菌器内装满培养基的锥形瓶,自下而上摆放。取5支经过校正的留点温度计,将其中1支的探头置于进气口处,1支探头置于排气口处,1支置于温度控制和记录的温度计旁边,其余的留点温度计均匀分布在腔内装载的各处。温度计分布情况同图1。
开启灭菌消毒器,按照121 ℃温度,运行30 min,且在运行过程中记录各个点的温度。连续运行3次,以检查其重现性,最低温度与最高温度之差应<2 ℃。
1.2.3 热穿透试验
将灭菌器内装满培养基的锥形瓶,自下而上摆放。取5支经过校正的留点温度计,将其中1支的探头置于进气口处,1支探头置于排气口处,1支置于温度控制和记录的温度计旁边,其余的留点温度计均匀分布在腔内装载的各处。温度计分布情况同图1。
开启灭菌消毒器,按照121 ℃温度,运行30 min,且在运行过程中记录各个点的温度。连续运行3次,以检查其重现性,最低温度与最高温度之差应<2 ℃。
1.2.3 热穿透试验
热穿透试验是在热分布试验的基础上,确定装载中的“最冷点”,并肯定该点在灭菌过程中获得的无菌保证值为121 ℃、≥30 min。
(1)灭菌程序:(121±2)℃×30 min。
(2)测试过程:选用500 ml锥型瓶(或90 mm培养碟)。在最大装载情况下,取5支经过校验的标准留点温度计,将其中3支分别置于进气口处的待灭菌瓶内、排气口处的待灭菌瓶内、灭菌器温度计测试点旁,其余温度计置于待灭菌瓶中,分布情况同图1。开启灭菌消毒器,按照温度121 ℃、运行30 min进行操作。
(3)生物指示剂实验:将一定量的耐热菌放入待灭菌的产品中,在设定的灭菌条件下进行灭菌,以验证设定的灭菌工艺是否确实赋予产品必须的灭菌值。
(4)验证选择:嗜热脂肪芽孢杆菌指示剂,含量1×106 CFU/支。
(5)验证方法:取嗜热脂肪芽孢杆菌指示剂,均匀分布于灭菌锅的各层位置,其中3支置于热穿透试验的最冷点,按照岗位SOP进行灭菌操作,温度为115~117 ℃,灭菌时间为30 min。经过一个灭菌周期后,取出嗜热脂肪芽孢杆菌指示剂,放入恒温培养箱中,在温度为55~60 ℃下培养48 h,观察嗜热脂肪芽孢杆菌指示剂的变色情况。同时将未灭菌的嗜热脂肪芽孢杆菌指示剂进行培养,作阳性对照。连续试验3次,每次检测中,每支嗜热脂肪芽孢杆菌指示剂呈蓝紫色为合格,指示剂之一呈黄色为不合格。
2 实验过程数据统计分析及结果
2.1 空载热分布实验
空载热分布实验数据统计分析情况如表1、表2所示。运行结果表明:灭菌器箱腔内的热分布均匀,符合规定。
表1 刚到121 ℃时各留点温度计温度
|
实验
次数 |
温度计编号及实验温度/ ℃ |
平均温度/ ℃ |
最大温差/ ℃ | ||||
|
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
Ⅴ | |||
|
第一次 |
120.8 |
120.7 |
120.9 |
121.0 |
120.9 |
120.9 |
0.3 |
|
第二次 |
120.9 |
120.9 |
120.8 |
120.9 |
121.0 |
120.9 | |
|
第三次 |
121.0 |
120.9 |
120.7 |
120.9 |
120.9 |
120.9 | |
表2 在121 ℃下稳定30 min时各留点温度计温度
|
实验
次数 |
温度计编号及实验温度/ ℃ |
温差/ ℃ | ||||
|
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
Ⅴ | ||
|
第一次 |
121.0 |
121.0 |
121.0 |
121.0 |
121.0 |
0 |
|
第二次 |
121.0 |
121.0 |
121.0 |
121.0 |
121.0 | |
|
第三次 |
121.0 |
121.0 |
121.0 |
121.0 |
121.0 | |
2.2 满载热分布实验
满载热分布实验数据统计分析情况如表3所示。运行结果表明:满载后箱内温度分布符合规定。
表3 满载热分布实验数据分析
|
实验
次数 |
温度计编号及实验温度/ ℃ |
温差/ ℃ | ||||
|
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
Ⅴ | ||
|
第一次 |
121.0 |
121.0 |
121.0 |
121.0 |
121.0 |
0 |
|
第二次 |
121.0 |
121.0 |
121.0 |
121.0 |
121.0 | |
|
第三次 |
121.0 |
121.0 |
121.0 |
121.0 |
121.0 | |
2.3 热穿透实验
热穿透实验数据统计分析情况如表4所示。运行结果表明:热穿透均匀,符合规定。
表4 热穿透实验数据分析
|
实验
次数 |
温度计编号及实验温度/℃ |
温差/℃ | ||||
|
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
Ⅴ | ||
|
第一次 |
122.0 |
122.0 |
122.0 |
122.0 |
122.0 |
0 |
|
第二次 |
122.0 |
122.0 |
122.0 |
122.0 |
122.0 | |
|
第三次 |
122.0 |
122.0 |
122.0 |
122.0 |
122.0 | |
2.4 生物指示剂试验结果
嗜热脂肪芽孢杆菌指示剂实验结果如表5所示。结果判定及评价:符合规定要求。
表5 嗜热脂肪芽孢杆菌指示剂实验结果
|
实验
次数 |
温度计编号及指示剂显示色 |
阳性对照品 | ||||
|
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
Ⅴ | ||
|
第一次 |
蓝紫色 |
蓝紫色 |
蓝紫色 |
蓝紫色 |
蓝紫色 |
黄色 |
|
第二次 |
蓝紫色 |
蓝紫色 |
蓝紫色 |
蓝紫色 |
蓝紫色 | |
|
第三次 |
蓝紫色 |
蓝紫色 |
蓝紫色 |
蓝紫色 |
蓝紫色 | |
2.5 灭菌后培养基质量验证
按照《微生物限度检查标准操作规程》规定的检查方法,从消毒后的培养基中每次取3瓶(分别从消毒器中不同位置)分别做碟,并同时做空白,在温度37 ℃下培养48 h,并记录菌落生长情况。具体情况如表6所示。验证结果:消毒器能确保物料灭菌合格,该高压消毒器能达到灭菌要求。
表6 灭菌前后菌落生长情况比较
|
实验
次数 |
平皿编号及个数 | |||||
|
Ⅰ |
Ⅱ |
Ⅲ | ||||
|
灭菌前 |
灭菌后 |
灭菌前 |
灭菌后 |
灭菌前 |
灭菌后 | |
|
第一次 |
45 |
0 |
43 |
0 |
44 |
0 |
|
第二次 |
48 |
0 |
45 |
0 |
45 |
0 |
|
第三次 |
51 |
0 |
47 |
0 |
46 |
0 |
3 讨论
(1)在高压蒸汽灭菌中,蒸汽是杀死细菌的介质,它灭菌的机制是使细菌中主要蛋白质及核酸变性。本次实验结果表明,在121 ℃的温度下蒸汽灭菌稳定30 min后,通过观察留点温度计的温度,消毒器内各个点温度恒定,从而确定其灭菌效果。不管是空载与满载情况下,高压蒸汽锅内当温度达到121 ℃稳定后不存在最冷点,温度分布均匀,并通过生物指示剂试验证明整个灭菌锅的灭菌效果符合要求。
(2)验证过程中的数据和分析内容应以文件形式归档保存,验证文件一般包括验证方案、验证报告、评价和建议、批准人等。当影响产品质量的主要因素,如工艺、质量控制方法、主要原辅料、主要生产设备等发生改变时,以及生产一定周期后,必须进行再验证。
4 结语
高压蒸汽灭菌验证是一项存在相当技术难度并需投入较大精力的方法验证,严谨、可靠的验证工作是产品质量的重要保证。实施本验证后可以避免由于灭菌不彻底而造成的不合格产品的产生,它所带来的效益要远远大于增加的成本。
[参考文献]
[1] 国家药品监督管理局.药品生产质量管理规范(1998)年修订[M].1999
[2] 中国化学制药工业协会等.药品生产质量管理规范实施指南[M].北京:化学工业出版社,2001